Cér je nesporným „veľkým bratom“ vo veľkej rodine prvkov vzácnych zemín. Po prvé, celkový výskyt prvkov vzácnych zemín v zemskej kôre je 238 ppm, pričom cér má 68 ppm, čo predstavuje 28 % celkového zloženia prvkov vzácnych zemín a je na prvom mieste; po druhé, cér je druhý prvok vzácnych zemín objavený deväť rokov po objavení ytria (1794). Jeho použitie je veľmi rozsiahle a „cér“ je nezastaviteľný.
Objav prvku céru

Carl Auer von Welsbach
Cér objavili a pomenovali v roku 1803 Nemec Kloppers, švédsky chemik Jöns Jakob Berzelius a švédsky mineralóg Wilhelm Hisinger. Nazýva sa cérium a jeho ruda sa nazýva cerit na pamiatku Ceres, asteroidu objaveného v roku 1801. V skutočnosti je tento typ kremičitanu céru hydratovaná soľ obsahujúca 66 % až 70 % céru, zatiaľ čo zvyšok tvoria zlúčeniny vápnika, železa a...ytrium.
Prvým použitím céru bol plynový krb, ktorý vynašiel rakúsky chemik Carl Auer von Welsbach. V roku 1885 sa pokúsil o zmes horčíka, lantánu a oxidu ytria, ale tieto zmesi neúspešne vyžarovali zelené svetlo.
V roku 1891 zistil, že čistý oxid tória produkuje lepšie svetlo, hoci je modré, a zmiešaním s oxidom céru(IV) vzniká jasné biele svetlo. Okrem toho sa oxid céru(IV) môže použiť aj ako katalyzátor spaľovania oxidu tória.
Cér kov

★ Cér je tvárny a mäkký striebornobiely kov s aktívnymi vlastnosťami. Pri vystavení vzduchu oxiduje a vytvára hrdzavú odlupujúcu sa oxidovú vrstvu. Pri zahrievaní horí a rýchlo reaguje s vodou. Vzorka kovového céru s veľkosťou centimetra úplne skoroduje približne do jedného roka. Zabráňte kontaktu so vzduchom, silnými oxidačnými činidlami, silnými kyselinami a halogénmi.
★ Cér sa vyskytuje najmä v monazite a bastnaezite, ako aj v štiepnych produktoch uránu, tória a plutónia. Škodlivý pre životné prostredie, preto by sa mala venovať osobitná pozornosť znečisťovaniu vodných útvarov.
★ Cér je 26. najrozšírenejší prvok, ktorý predstavuje 68 ppm zemskej kôry, druhý hneď po medi (68 ppm). Cér je zastúpený vo väčšom množstve ako bežné kovy, ako je olovo (13 ppm) a cín (2,1 ppm).
Konfigurácia elektrónov céru
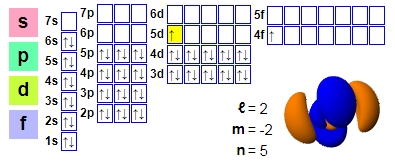
Elektronické dojednania:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f1 5d1
★ Cér sa nachádza za lantánom a má 4f elektróny začínajúce od céru, čo mu uľahčuje účasť na chemických reakciách. 5d orbital céru je však obsadený a tento efekt nie je v cériu dostatočne silný.
★ Väčšina lantanoidov dokáže ako valenčné elektróny použiť iba tri elektróny, s výnimkou céru, ktorý má variabilnú elektronickú štruktúru. Energia 4f elektrónov je takmer rovnaká ako energia externých 5d a 6s elektrónov delokalizovaných v kovovom stave a na zmenu relatívneho obsadenia týchto elektrónových energetických hladín je potrebné len malé množstvo energie, čo vedie k dvojitej valencii +3 a +4. Normálny stav je valencia +3, čo v anaeróbnej vode vykazuje valenciu +4.
Aplikácia céru

★ Môže sa použiť ako prísada do zliatin a na výrobu cérových solí atď.
★ Môže sa použiť ako prísada do skla na absorbovanie ultrafialového a infračerveného žiarenia a je široko používaný v automobilovom skle.
★ Môže sa použiť ako vynikajúci materiál na ochranu životného prostredia a v súčasnosti je najreprezentatívnejším katalyzátorom na čistenie výfukových plynov automobilov, ktorý účinne zabraňuje vypúšťaniu veľkého množstva výfukových plynov automobilov do ovzdušia.
★ Svetloprvky vzácnych zemínprevažne zložené z céru ako regulátorov rastu rastlín môžu zlepšiť kvalitu plodín, zvýšiť výnosy a zvýšiť odolnosť plodín voči stresu.
★ Sulfid céru môže nahradiť kovy ako olovo a kadmium, ktoré sú škodlivé pre životné prostredie a ľudí v pigmentoch, môže farbiť plasty a môže sa použiť aj v priemysle náterov a atramentov.
★Oxid céru(IV)môže sa použiť ako leštiaca pasta, napríklad pri chemicko-mechanickom leštení (CMP).
★ Cér sa môže použiť aj ako materiál na ukladanie vodíka, termoelektrické materiály, cérovo-volfrámové elektródy, keramický kondenzátor, piezoelektrická keramika, cérovo-kremíkové abrazíva, suroviny pre palivové články, benzínové katalyzátory, permanentné magnetické materiály, zdravotnícke materiály, rôzne legované ocele a neželezné kovy.
Čas uverejnenia: 3. júla 2023