Prazeodýmje tretím najrozšírenejším lantanoidovým prvkom v periodickej tabuľke chemických prvkov s výskytom 9,5 ppm v zemskej kôre, čo je len menej akocér, ytrium,lantánaskandiumJe to piaty najrozšírenejší prvok medzi vzácnymi zeminami. Ale rovnako ako jeho meno,prazeodýmje jednoduchý a nezdobený člen rodiny vzácnych zemín.
Prazeodým objavil C. F. Auer von Welsbach v roku 1885.
V roku 1751 objavil švédsky mineralóg Axel Fredrik Cronstedt v banskej oblasti Bastnäs ťažký minerál, ktorý bol neskôr pomenovaný cerit. O tridsať rokov neskôr poslal pätnásťročný Vilhelm Hisinger z rodiny, ktorá vlastnila baňu, svoje vzorky Carlovi Scheelemu, ale ten neobjavil žiadne nové prvky. V roku 1803, keď sa Singer stal kováčom, sa vrátil do banskej oblasti s Jönsom Jacobom Berzeliusom a oddelili nový oxid, trpasličiu planétu Ceres, ktorú objavili pred dvoma rokmi. Cér nezávisle od seba oddelil Martin Heinrich Klaproth v Nemecku.
Medzi rokmi 1839 a 1843 švédsky chirurg a chemik Carl Gustaf Mosander zistil, žeoxid cérubola zmesou oxidov. Oddelil dva ďalšie oxidy, ktoré nazval lantán a didymia „didymia“ (čo v gréčtine znamená „dvojčatá“). Čiastočne rozložildusičnan céruvzorku pražením na vzduchu a následným spracovaním zriedenou kyselinou dusičnou za vzniku oxidu. Kovy, ktoré tvoria tieto oxidy, sa preto nazývajúlantánaprazeodým.
V roku 1885 Rakúšan CF Auer von Welsbach, ktorý vynašiel gázový kryt pre tóriovo-cérovú lampu, úspešne oddelil „prazeodýmový neodým“, „siamské dvojčatá“, z ktorých sa oddelila zelená prazeodýmová soľ a ružová neodýmová soľ, ktoré boli určené ako dva nové prvky. Jeden sa nazýva „prazeodým“, čo pochádza z gréckeho slova prason, čo znamená zelená zlúčenina, pretože roztok prazeodýmovej soli vo vode bude mať jasne zelenú farbu; druhý prvok sa nazýva „Neodým„Úspešné oddelenie „siamských dvojčiat“ im umožnilo nezávisle prejaviť svoj talent.“
Striebornobiely kov, mäkký a tvárny. Prazeodým má pri izbovej teplote hexagonálnu kryštálovú štruktúru. Odolnosť voči korózii na vzduchu je silnejšia ako u lantánu, céru, neodýmu a európia, ale pri vystavení vzduchu sa vytvorí vrstva krehkého čierneho oxidu a vzorka kovového prazeodýmu s veľkosťou jeden centimeter úplne skoroduje do približne jedného roka.
Ako väčšinaprvky vzácnych zemínPrazeodým s najväčšou pravdepodobnosťou tvorí oxidačný stav a+3, čo je jeho jediný stabilný stav vo vodných roztokoch. Prazeodým sa v niektorých známych pevných zlúčeninách vyskytuje v oxidačnom stave a+4 a za podmienok matricovej separácie môže dosiahnuť jedinečný oxidačný stav +5 medzi lantanoidovými prvkami.
Vodný prazeodýmový ión je chartreuse a mnohé priemyselné využitia prazeodýmu zahŕňajú jeho schopnosť filtrovať žlté svetlo vo svetelných zdrojoch.
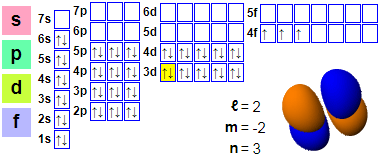
Elektronické rozloženie s prazeodýmom
Elektronické emisie:
1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p66s2 4f3
59 elektrónov prazeodýmu je usporiadaných ako [Xe] 4f36s2. Teoreticky sa všetkých päť vonkajších elektrónov môže použiť ako valenčný elektrón, ale použitie všetkých piatich vonkajších elektrónov vyžaduje extrémne podmienky. Prazeodým vo svojich zlúčeninách vo všeobecnosti emituje iba tri alebo štyri elektróny. Prazeodým je prvý lantanoidový prvok s elektronickou konfiguráciou, ktorá zodpovedá Aufbauovmu princípu. Jeho 4f orbitál má nižšie energetické hladiny ako 5d orbitál, čo sa nedá aplikovať na lantán a cér, pretože k náhlej kontrakcii 4f orbitalu nedochádza skôr ako po lantáne a nie je dostatočná na to, aby sa zabránilo obsadeniu 5d vrstvy v cériu. Napriek tomu tuhý prazeodým vykazuje konfiguráciu [Xe] 4f25d16s2, kde jeden elektrón v 5d vrstve pripomína všetky ostatné trojmocné lantanoidové prvky (okrem európia a yterbia, ktoré sú v kovovom stave dvojmocné).
Tak ako väčšina lantanoidových prvkov, aj prazeodým zvyčajne používa ako valenčné elektróny iba tri elektróny a zvyšné 4f elektróny majú silný väzbový účinok: je to preto, že 4f orbita prechádza cez inertné xenónové jadro elektrónu, aby dosiahla jadro, nasledované 5d a 6s, a zvyšuje sa so zvyšujúcim sa iónovým nábojom. Prazeodým však môže stále strácať štvrtý a dokonca príležitostne aj piaty valenčný elektrón, pretože sa objavuje veľmi skoro v lantanoidovom systéme, kde je jadrový náboj stále dostatočne nízky a energia 4f podvrstvy je dostatočne vysoká, aby umožnila odstránenie väčšieho množstva valenčného elektrónu.
Prazeodým a všetky lantanoidové prvky (okremlantán, yterbiumalutécium, neexistujú žiadne nepárové 4f elektróny) sú paramagnetistické pri izbovej teplote. Na rozdiel od iných kovov vzácnych zemín, ktoré vykazujú antiferomagnetické alebo feromagnetické usporiadanie pri nízkych teplotách, prazeodým je paramagnetistický pri všetkých teplotách nad 1 K.
Aplikácia praseodýmu
Prazeodým sa väčšinou používa vo forme zmesí vzácnych zemín, napríklad ako čistiace a modifikačné činidlo pre kovové materiály, chemické katalyzátory, poľnohospodárske vzácne zeminy atď.Prazeodým neodýmje najpodobnejší a najťažšie oddeliteľný pár prvkov vzácnych zemín, ktorý je ťažké oddeliť chemickými metódami. Priemyselná výroba zvyčajne využíva metódy extrakcie a iónovej výmeny. Ak sa používajú v pároch vo forme obohateného prazeodýmu neodýmu, možno plne využiť ich spoločné vlastnosti a cena je tiež nižšia ako u produktov s jedným prvkom.
Zliatina prazeodýmu a neodýmu(prazeodým (neodýmový kov)sa stal nezávislým produktom, ktorý sa môže použiť ako materiál pre permanentné magnety aj ako modifikačná prísada pre zliatiny neželezných kovov. Aktivitu, selektivitu a stabilitu katalyzátora krakovania ropy je možné zlepšiť pridaním koncentrátu praseodýmu a neodýmu do molekulového sita zeolitu Y. Ako modifikačná prísada pre plasty môže pridanie obohatenia praseodýmom a neodýmom do polytetrafluóretylénu (PTFE) výrazne zlepšiť odolnosť PTFE proti opotrebeniu.
Vzácna zemMateriály s permanentnými magnetmi sú v súčasnosti najobľúbenejšou oblasťou aplikácií vzácnych zemín. Prazeodým sám o sebe nie je vynikajúci ako materiál s permanentnými magnetmi, ale je to vynikajúci synergický prvok, ktorý môže zlepšiť magnetické vlastnosti. Pridanie vhodného množstva prazeodýmu môže účinne zlepšiť výkon materiálov s permanentnými magnetmi. Môže tiež zlepšiť antioxidačné vlastnosti (odolnosť proti korózii na vzduchu) a mechanické vlastnosti magnetov a široko sa používa v rôznych elektronických zariadeniach a motoroch.
Prazeodým sa môže použiť aj na brúsenie a leštenie materiálov. Ako všetci vieme, leštiaci prášok na báze čistého céru je zvyčajne svetložltej farby a je vysoko kvalitným leštiacim materiálom pre optické sklo. Nahradil červený prášok oxidu železa, ktorý má nízku leštiacu účinnosť a znečisťuje výrobné prostredie. Ľudia zistili, že prazeodým má dobré leštiace vlastnosti. Leštiaci prášok na vzácne zeminy obsahujúci prazeodým sa javí ako červenohnedý, tiež známy ako „červený prášok“, ale táto červená farba nie je červená oxidu železa, ale kvôli prítomnosti oxidu prazeodýmu sa farba leštiaceho prášku na vzácne zeminy stáva tmavšou. Prazeodým sa tiež používa ako nový brúsny materiál na výrobu korundových brúsnych kotúčov obsahujúcich prazeodým. V porovnaní s bielym oxidom hlinitým sa môže účinnosť a trvanlivosť zlepšiť o viac ako 30 % pri brúsení uhlíkovej konštrukčnej ocele, nehrdzavejúcej ocele a vysokoteplotných zliatin. Aby sa znížili náklady, v minulosti sa ako surovina často používali materiály obohatené prazeodýmom a neodýmom, odtiaľ pochádza názov prazeodýmový neodýmový korundový brúsny kotúč.
Kryštály kremičitanu dopované iónmi prazeodýmu sa používajú na spomalenie svetelných impulzov na niekoľko stoviek metrov za sekundu.
Pridaním oxidu prazeodýmu do kremičitanu zirkoničitého sa farba zmení na jasne žltú a môže sa použiť ako keramický pigment – prazeodýmová žltá. Prazeodýmová žltá (Zr02-Pr6Oll-Si02) sa považuje za najlepší žltý keramický pigment, ktorý zostáva stabilný až do 1000 ℃ a môže sa použiť na jednorazové použitie alebo na opätovné vypaľovanie.
Prazeodým sa tiež používa ako farbivo na sklo so sýtymi farbami a veľkým potenciálnym trhom. Z prazeodýmu sa dajú vyrobiť sklenené výrobky s jasnou pórovozelenou a jarnozelenou farbou, ktoré sa dajú použiť na výrobu zelených filtrov a tiež na umelecké a remeselné sklo. Pridaním oxidu prazeodýmu a oxidu céru do skla sa dajú vyrobiť ochranné okuliare na zváranie. Sulfid prazeodýmu sa môže použiť aj ako zelené farbivo na plasty.
Čas uverejnenia: 29. mája 2023